EL ÁTOMO
La Química actual descansa sobre el concepto de átomo como unidad de materia que se conserva en las reacciones químicas. Los átomos pueden combinarse entre sí para formar moléculas, iones y otras entidades, generando así distintas sustancias. Pero, ¿Cómo se define actualmente el concepto de átomo? Veamos aquí los problemas que plantea esta definición.
El término átomo fue introducido en el siglo V a. C. por Leucipo como “la partícula indivisible más pequeña de materia“. Sin embargo, la definición de Leucipo no coincide con el concepto actual de átomo químico. Así, un átomo está formado por electrones y un núcleo, que a su vez está formado por partículas subatómicas (protones y neutrones), que a su vez están formadas por quarks (estos sí son partículas elementales, según el Modelo Estándar de la Física de partículas). Así pues, los átomos de Leucipo no corresponderían en realidad a los átomos actuales, sino a los fermiones, tanto quarks como electrones.
ESTRUCTURA DEL ÁTOMO
El átomo está compuesto por tres subpartículas:
Protones, con carga positiva.
Neutrones, sin carga eléctrica (o carga neutra).
Electrones, con carga negativa.
A su vez, se divide en dos partes:
El núcleo. Formado por neutrones y protones.
La corteza. Formada únicamente por electrones.
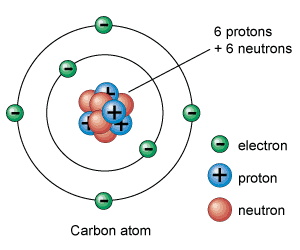
Los protones, neutrones y electrones son las partículas subatómicas que forman la estructura atómica. Lo que les diferencia entre ellos es la relación que se establecen entre ellas.
Los electrones son las partículas subatómicas más ligeras. Los protones, de carga positiva, pesan unas 1.836 veces más que los electrones. Los neutrones, los únicos que no tienen carga eléctrica, pesan aproximadamente lo mismo que los protones.
Los protones y neutrones se encuentran agrupados en el núcleo atómico. Por este motivo también se les llama nucleones. La energía que mantiene unidos los protones y los neutrones es la energía nuclear.
Por lo tanto, el núcleo atómico, tiene una carga positiva (la de los protones) en la que se concentra casi toda su masa.
Por otra parte, alrededor del núcleo hay un cierto número de electrones, cargados negativamente. La carga total del núcleo (positiva) es igual a la carga negativa de los electrones, de modo que la carga eléctrica total es neutra.
SESIÓN 2
1. https://phet.colorado.edu/sims/html/build-an-atom/latest/build-an-atom_es.html
2.

No hay comentarios:
Publicar un comentario